Rumus kalor adalah hal yang tidak asing lagi ditemukan dalam pelajaran Fisika. Kalor sendiri merupakan salah satu bentuk energi yang dapat diterima atau dilepaskan oleh suatu benda. Kalor memiliki satuan bernama joule atau kalori.
Kalor dapat diartikan sebagai energi panas yang dimiliki oleh zat tertentu, dan dapat dideteksi dengan alat pengukur suhu benda itu. Kamu dapat melihat aplikasi kalor pada air hangat yang dibiarkan terbuka, lama-kelamaan mendingin (tidak menghangat lagi) karena kalor dilepaskan dari air ke udara.
Daftar Isi
Pengertian Kalor

Kalor merupakan suatu energi yang dapat berpindah dari suatu benda bersuhu lebih tinggi menuju benda yang bersuhu lebih rendah apabila kedua benda tersebut saling bersentuhan atau dipertemukan. Kedua benda dengan suhu berbeda akan menyebabkan kalor mengalir dan berpindah.
Misalnya, ketika kamu mencampurkan air panas dan air dingin, air yang bergabung akan menjadi air hangat. Kamu juga harus memahami bahwa suhu dan kalor adalah dua hal berbeda. Suhu merupakan nilai yang dapat diukur dengan termometer, sementara kalor adalah energi yang mengalir.
Menurut Sistem Internasional (SI) atau MKS, satuan kalor adalah Joule (J), sementara menurut CGS satuan kalor adalah erg. Untuk sejumlah jenis makanan, kalor memakai satuan kalori.
Satu kalori diartikan sebagai banyaknya energi panas yang diperlukan untuk menaikkan suhu 1 gram air menjadi 1 derajat Celcius. Maka, dapat disimpulkan bahwa 1 kalori = 4,184 Joule atau umumnya langsung dibulatkan menjadi 4,2 J.
Rumus Kalor
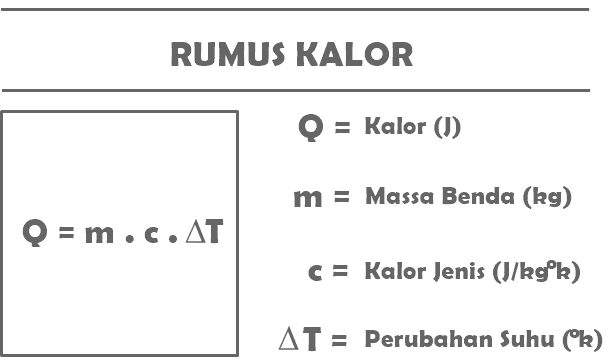
Menurut pengertian kalor yang sudah kamu baca di atas, berikut ini adalah beberapa rumus-rumus yang sudah dirangkum yang berkaitan dengan materi kalor dalam mata pelajaran Fisika.
1. Rumus Perpindahan Kalor
Q = m . c . ΔT
Dengan:
Q = banyak kalor yang diterima atau dilepas oleh suatu benda tertentu (J)
m = massa benda yang menerima atau melepas kalor (kg)
c = kalor jenis zat (J/kg°C)
ΔT = perubahan suhu (°C)
2. Rumus Kalor Jenis
Patokan rumus ini adalah rumus perpindahan kalor, dengan mengeluarkan unsur c (kalor jenis zat) untuk dihitung secara matematis seperti biasa.
c = Q / (m . ΔT)
Dengan:
c = kalor jenis zat (J/kg°C)
Q = banyak kalor yang diterima atau dilepas oleh suatu benda tertentu (J)
m = massa benda yang menerima atau melepas kalor (kg)
ΔT = perubahan suhu (°C)
3. Rumus Kapasitas Kalor
C = Q / ΔT
Dengan:
C = kapasitas kalor (J/°K)
Q = banyak kalor (J)
ΔT = perubahan suhu (Kelvin / K)
4. Rumus Menentukan Kapasitas Kalor
C = m . c
Dengan:
C = kapasitas kalor (J/°K)
m = massa benda yang menerima atau melepas kalor (kg)
c = kalor jenis zat (J/kg°K)
5. Rumus Kalor Lebur dan Uap
Rumus untuk kalor lebur adalah sebagai berikut.
Q = m . L
Rumus untuk kalor uap adalah sebagai berikut.
Q = m . U
Dengan:
Q = banyak kalor (J)
m = massa benda (kg)
L = kalor lebur zat (J/kg)
U = kalor uap zat (J/kg)
Baca: Termodinamika
Jenis-Jenis Kalor

Ada beberapa jenis kalor yang dibedakan berdasarkan proses kerjanya pada suatu zat tertentu. Di bawah ini adalah jenis-jenis kalor yang perlu kamu pahami untuk dapat melihat aplikasinya pada kehidupan sehari-hari.
1. Kalor Pembentukan (ΔHf)
Kalor pembentukan merupakan kalor yang dihasilkan atau diperlukan untuk membentuk 1 mol senyawa dalam unsur-unsurnya, seperti gas yang ditulis memakai rumus molekul. Beberapa contoh kalor pembentukan adalah C12, O2, Br2, H2.
2. Kalor Penguraian (ΔHd)
Kalor penguraian merupakan bentuk kalor yang dihasilkan atau diperlukan untuk mengurai 1 mol senyawa menjadi unsur lain.
3. Kalor Pembakaran (ΔHc)
Kalor pembakaran merupakan kalor yang diperoleh atau dibutuhkan untuk membakar 1 mol zat, seperti unsur atau senyawanya.
4. Kalor Netralisasi (ΔHn)
Kalor netralisasi merupakan jenis kalor yang diperoleh atau diperlukan untuk membentuk satu mol H2O dari reaksi antara asam dan basa. Kalor ini merupakan reaksi eksoterm sebab terdapat reaksi kenaikan suhu.
5. Kalor Pelarutan (ΔHs)
Kalor pelarutan merupakan jenis kalor yang dihasilkan atau diperlukan untuk melarutkan 1 mol zat yang semula padat menjadi bentuk larutan.
Baca: Rumus Massa Jenis
Kalor Jenis dan Kapasitas Kalor
Kamu juga perlu mengetahui bahwa kalor dapat mengalir pada dua zat yang memiliki partikel zat berbeda dan perubahan suhu yang berbeda. Misalnya, ketika air dan minyak dipanaskan dalam suhu sama, maka suhu minyak berubah lebih besar daripada perubahan suhu air.
Hal tersebut dapat terjadi oleh sebab terdapat kalor jenis yang berbeda pada dua benda yang dipertemukan atau disatukan. Kalor jenis merupakan banyak kalor yang dibutuhkan untuk menaikkan suhu dari 1 kg massa menjadi 1°C, satuannya adalah kalori/gram°Celcius atau J/kg°C.
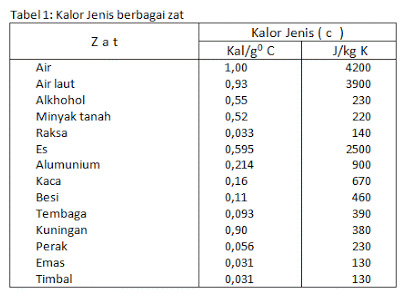
Tiap-tiap zat benda mempunyai kalor jenis masing-masing dan ada perbedaan di dalamnya. Sementara itu, pengertian kapasitas kalor adalah jumlah kalor yang diperlukan atau diserap untuk dapat menaikkan suhu suatu benda menjadi 1°C.
Perubahan Kalor
Dalam aplikasinya, rumus kalor bekerja memakai prinsip yang mengubah dua zat yang dipertemukan atau saling bersentuhan. Di bawah ini merupakan perubahan kalor yang terjadi jika ada zat-zat benda yang disatukan atau dipertemukan.
1. Kalor Dapat Mengubah Suhu Zat
Tiap-tiap benda dasarnya mempunyai suhu yang lebih rendah daripada nol mutlak, sehingga benda tersebut sudah pasti memiliki kalor. Kandungan tersebut nantinya akan menjadi penentu sebanyak apa kalor yang dimiliki suhu benda itu.
Apabila benda itu dipanaskan, maka dia akan mendapatkan tambahan kalor. Suhunya pun akan bertambah atau meningkat. Sebaliknya, apabila benda itu didinginkan, maka kalor akan dilepaskan dan menyebabkan penurunan suhu.
2. Kalor Dapat Mengubah Wujud Zat
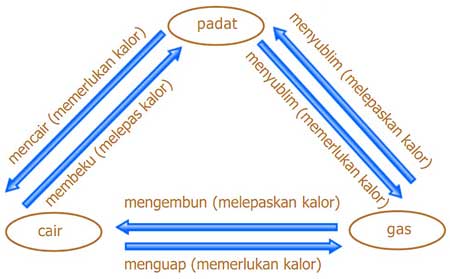
Pada beberapa jenis benda, apabila diberikan kalor dalam satuan tertentu, benda itu dapat mengalami perubahan wujud. Misalnya, jika es diberi kalor (dipanaskan) maka es itu akan berubah wujud dari padat menjadi cair atau bahkan bentuk gas.
Apabila proses pemanasan dilakukan secara berkelanjutan, hal itulah yang menyebabkan air akan berubah wujud kembali menjadi zat. Hal itu terjadi saat benda yang akan berubah wujud bergerak dari titik zat cair menjadi titik lebur zat benda tersebut.
Macam-Macam Perpindahan Kalor
Sesudah melewati penjelasan mengenai pengertian, jenis, rumus kalor, hingga perubahan kalor, kamu dapat menyimpulkan bahwa kalor juga dapat berpindah ketika bertemu atau bersentuhan dengan benda lain. Berikut ini adalah beberapa jenis perpindahan kalor.
1. Konduksi
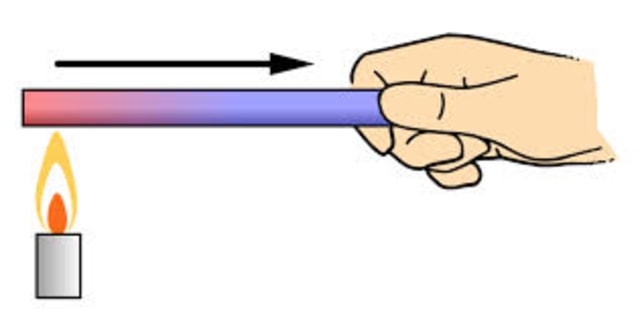
Perpindahan kalor secara konduksi terjadi ketika melalui zat perantara seperti logam, tetapi tidak diikuti dengan perpindahan partikel-partikel secara permanen pada zat tersebut. Misalnya, saat memanaskan ujung logam, ujung logam lain akan panas juga.
Hal tersebut ada oleh sebab hantaran kalor dari suhu tinggi ke suhu yang lebih rendah. Ujung logam yang dipanaskan akan menyebabkan partikel logam menciptakan getaran pada partikel lain yang terkoneksi dengannya.
Karena itu, semua partikel logam bergetar walau hanya satu bagian ujung logam yang dipanaskan, untuk kemudian menyebabkan adanya perpindahan kalor. Contoh lain ialah ketika knalpot sepeda motor yang panas saat motor dinyalakan.
Konduksi juga terjadi ketika kamu memegang kembang api yang dibakar, memegang tutup panci yang terasa panas ketika proses memasak, mentega yang meleleh ketika dipanaskan, dan lain sebagainya. rumus kalor yang berpindah untuk konduksi adalah sebagai berikut.
Laju Kalor = Q/t = kA . ΔT / x
2. Konveksi
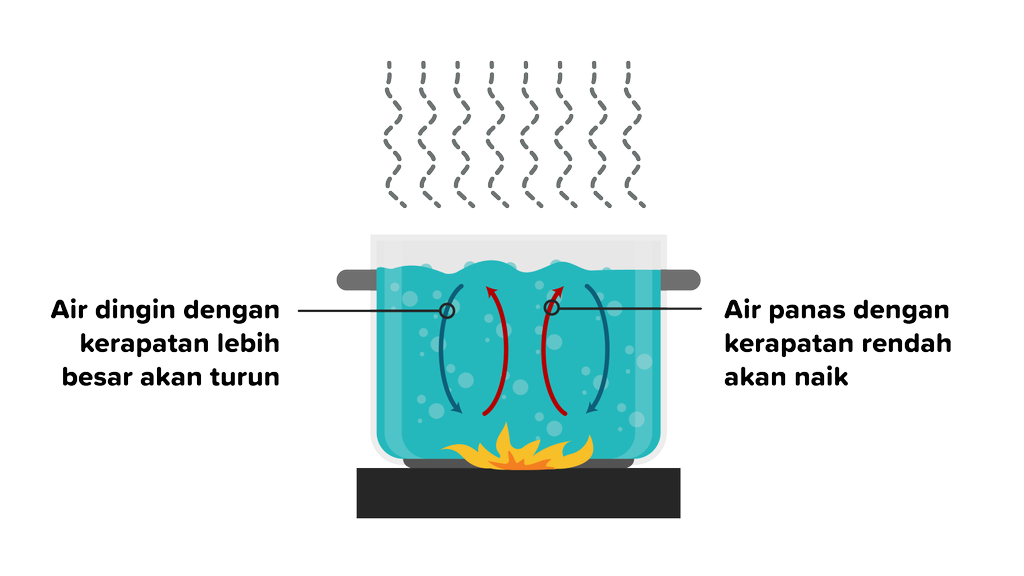
Konveksi merupakan perpindahan kalor di mana kalor melalui suatu zat dan diikuti dengan perpindahan bagian-bagian zat tersebut. Perpindahan kalor secara konveksi dapat terjadi pada zat cair atau gas, sehingga konveksi terbagi menjadi dua seperti berikut.
a. Konveksi Secara Ilmiah
Konveksi ini merupakan perpindahan kalor yang terjadi karena gaya apung tanpa faktor luar serta dipengaruhi oleh perbedaan jenis benda. Contoh kasusnya adalah ketika memanaskan air, massa jenis partikel air yang panas akan menjauh dari api, lalu zat air bersuhu lebih rendah akan menggantikan.
b. Konveksi Paksa
Konveksi ini merupakan perpindahan kalor yang disebabkan oleh pengaruh faktor luar, misalnya tekanan, sehingga perpindahan terjadi secara sengaja atau dipaksa. Artinya, kalor dipaksa untuk berpindah menuju suatu tempat karena adanya bantuan.
Contoh kasusnya adalah ketika kipas angin yang menghasilkan udara dingin ke suatu tempat yang terasa panas, adanya sistem pendingin mesin pada radiator mobil, dan sebagainya.
Penerapan konveksi yang lain terjadi saat pemanasan air, di mana terdapat gerakan naik-turun air, biji kacang hijau yang naik-turun ketika direbus, proses terjadinya angin darat dan angin laut, gerakan balon udara, asap cerobong pabrik.
Rumus kalor yang berpindah secara konveksi adalah sebagai berikut.
Laju Kalor = Q/t = hA . ΔT
3. Radiasi

Radiasi adalah perpindahan kalor yang tidak memerlukan zat atau media perantara. Perpindahan kalor dalam radiasi tidak sama dengan konduksi dan konveksi. Perpindahan dalam radiasi tidak selalu membuat kedua zat bersentuhan atau bertemu, sebab kalor dapat berpindah bahkan tanpa perantara.
Artinya, kalor akan dipancarkan ke segala arah oleh sumber panas itu sendiri, lalu mengalir ke segala arah yang dapat dicapai. Pada dasarnya, semua benda bisa memancarkan dan menyerap radiasi kalor, tetapi besarnya tergantung pada suhu dan warna zat tersebut.
Makin panas benda daripada suhu di sekitarnya, maka makin besar pula kalor yang diradiasikan ke lingkungannya. Jadi, apabila luas permukaan benda panas semakin besar, kalor yang akan diradiasikan akan semakin panas.
Contoh kasus radiasi dalam kehidupan sehari-hari adalah ketika kamu membuat api unggun, maka akan terasa hangat karena sumber api yang ada di jarak tertentu, radiasi terasa ketika telapak tangan menjadi hangat saat didekatkan dengan api. Rumus kalor untuk radiasi adalah sebagai berikut.
Laju Kalor = Q/t = eσAT4
4. Mengisolasi Kalor
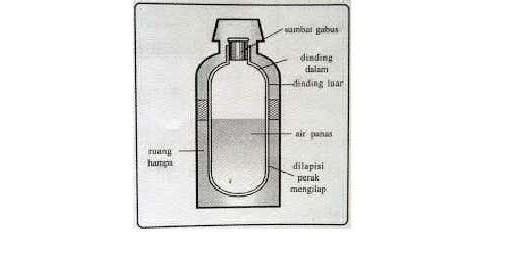
Kalor memiliki sifat yang mudah berpindah. Kamu dapat mencegah agar perpindahan tidak terjadi, baik itu secara konduksi, konveksi, dan radiasi. Misalnya dengan mengisolasi ruangan; termos dapat menjaga suhu air tetap panas atau hangat, sehingga perpindahan kalor dapat dicegah.
Baca: Zat Gas
Contoh Soal Kalor

Rumus kalor adalah cara yang dapat kamu gunakan untuk mengerjakan contoh-contoh soal berikut ini!
1. Contoh Soal 1
Suatu benda memiliki suhu 5°C, kemudian menyerap kalor sebanyak 1500 J. Suhu benda berubah menjadi 32°C. Hitung kapasitas kalor benda itu!
Penyelesaian:
Q = 1500 J
ΔT = 32°C – 5°C = 27°C = 300°K
C = Q / ΔT
C = 1500 / 300
C = 5 J/°K
2. Contoh Soal 2
Hitung kalor yang diperlukan untuk memanaskan 5 kg air bersuhu 25°C menjadi 105°C apabila diketahui bahwa kalor jenis air adalah 1000 J/kg°C!
Penyelesaian:
m = 5 kg
c = 1000 J/kg°C
ΔT = 105°C – 25°C = 80°C
Q = m . c. ΔT
Q = 5 . 1000 . 80
Q = 400.000 J
3. Contoh Soal 3
Apabila suatu air memiliki massa 3 kg dan dipanaskan dari suhu 30°C menjadi 100°C dan kalor jenisnya adalah 1 J/g°C, hitunglah besaran kalor yang diperlukan air tersebut!
Penyelesaian:
m = 3 kg
c = 1 g/°C = 1000 J/kg°C
ΔT = 100°C – 30°C = 70°C
Q = m . c . ΔT
Q = 3 . 1000 . 70
Q = 210.000 J
4. Contoh Soal 4
Suatu zat cair memiliki massa sebesar 5 kg. Zat cair itu membutuhkan kalor 200.000 J, dan dipanaskan dari suhu 20°C sampai menjadi 80°C. Hitung kalor jenis zat cair tersebut!
Penyelesaian:
m = 5 kg
Q = 200.000 J
ΔT = 80°C – 20°C = 60°C
c = Q / m . ΔT
c = 200.000 / 5 . 60
c = 200.000 / 300
c = 666,67 J/kg°C
5. Contoh Soal 5
Suatu aluminium memiliki massa 5 kg. Suhu awalnya adalah 25°C. Apabila aluminium tersebut menerima kalor sebanyak 250.000 J dan kalor jenisnya adalah 900 J/kg°C, hitunglah suhu akhir aluminium tersebut!
Penyelesaian:
m = 5 kg
Q = 250.000 J
c = 900 J/kg°C
T1 = 25°C
Q = m . c . ΔT
250.000 = 5 . 900 . (T2 – 25)
T2 – 25 = 250.000 / 5 . 900
T2 – 25 = 250.000 / 4.500
T2 – 25 = 55,56
T2 = 55,56 + 25 = 80,56°C
6. Contoh Soal 6
Terdapat air sebanyak 300 gram dengan suhu 25°C, akan dipanaskan dengan energi sebesar 1.500 kalori. Apabila kalor jenis air adalah 1 kal/g°C, hitung suhu air setelah dipanaskan!
Penyelesaian:
m = 300 gram
T1 = 25°C
c = 1 kal/g°C
Q = 1.500 kal
Q = m . c. ΔT
1.500 = 300 . 1 . (T2 – 25)
T2 – 25 = 1500 / 300 . 1
T2 – 25 = 5
T2 = 5 + 25 = 30°C
7. Contoh Soal 7
Terdapat 300 gram air yang akan dipanaskan dari suhu 40°C menjadi 65°C. Apabila kalor jenis air adalah 1 kal/g°C atau 4.200 J/kg°K, hitunglah:
- Banyak kalor yang diterima dalam kalori
- Banyak kalor yang diterima dalam Joule
Penyelesaian:
m = 300 g = 0,3 kg
ΔT = 65 – 40 = 25°C
c = 1 kal/g°C = 4.200 J/kg°K
- Kalor dalam kalori
Q = m . c . ΔT
Q = 300 . 1 . 25
Q = 7.500 kalori
- Kalor dalam Joule
Q = m . c . ΔT
Q = 0,3 . 4.200 . 25
Q = 31.500 kalori = 132.300 Joule
Berdasarkan penjelasan di atas, rumus kalor tidak hanya berputar pada melepaskan dan membutuhkan kalor, tetapi terdapat perubahan kalor, perpindahan kalor, bahkan kalor jenis tiap zat yang berbeda-beda. Selamat berlatih dan semoga tulisan ini bermanfaat!