Elektron valensi merupakan elektron yang berada di tingkat terluar atom yang bisa berpartisipasi dalam interaksi terhadap atom lainnya. Nilai valensi dapat mewakili sebuah atom sehingga nilai interaksinya dapat terlihat.
Jumlah valensi yang terdapat pada atom bisa menyebabkan sebuah unsur dapat reaktif maupun non aktif. Untuk itu sangatlah penting mengetahui jumlah valensi untuk dapat mengetahui keaktifan sebuah unsur terkait.
Daftar Isi
Pengertian Elektron Valensi
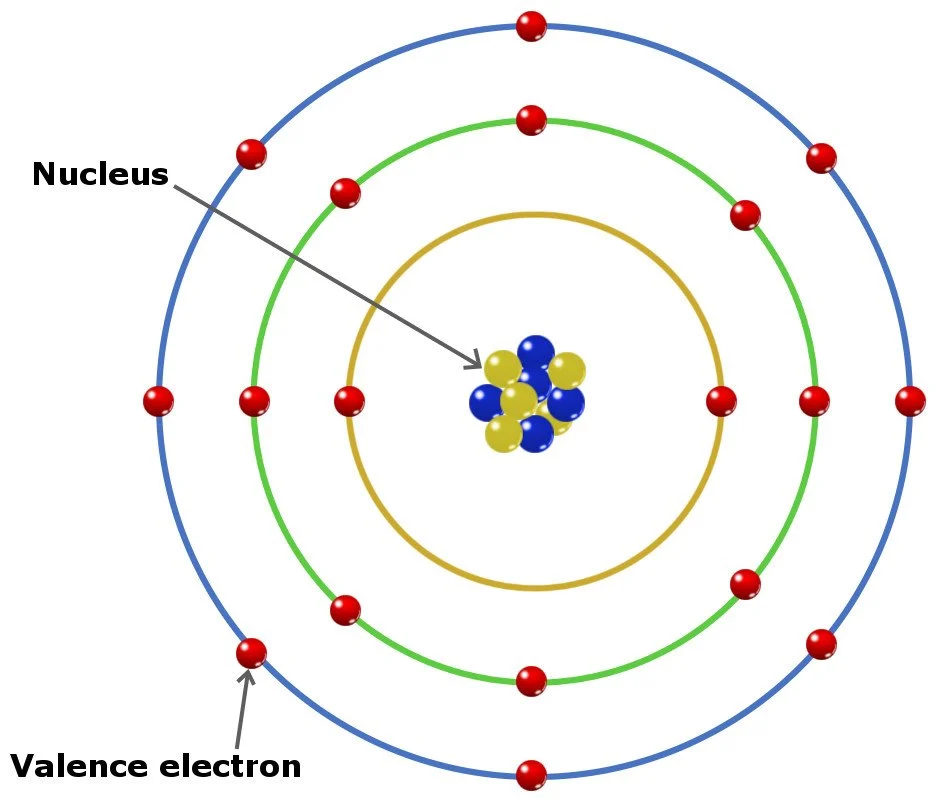
Elektron valensi dalam atom dapat berperan untuk membentuk suatu ikatan kimia pada sebuah unsur. Pada unsur yang terdapat pada golongan utama, valensi adalah elektron yang terdapat pada bagian kulit terluar.
Meskipun seperti itu, namun tidak semua jenis elektron ini berada di kulit terluar. Pada beberapa unsur yang termasuk dalam golongan transisi, valensi berada lebih dalam daripada kulit bagian terluar.
Baca: Konfigurasi Elektron
Tabel Elektron Valensi
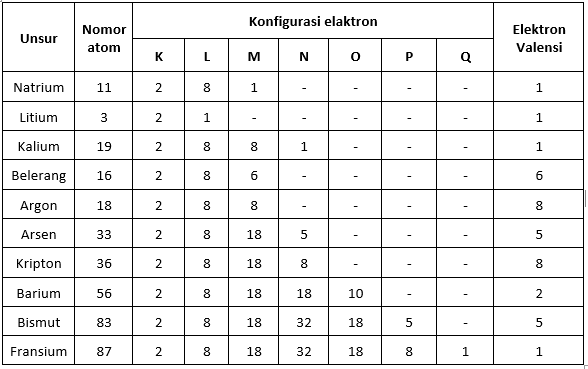
Elektron Valensi dan Sistem Periodik Unsur
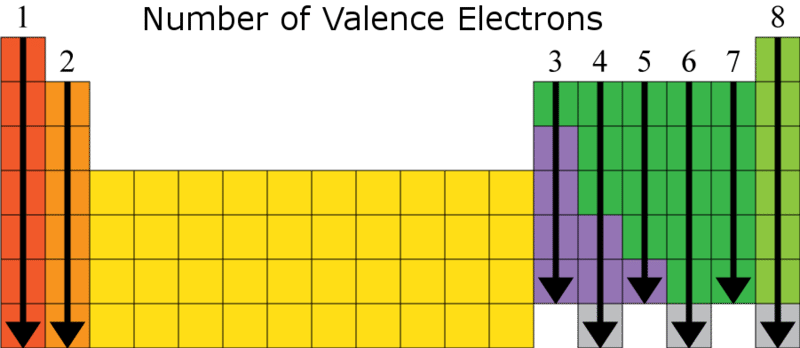
Sifat dari suatu unsur sangat bergantung terhadap konfigurasi elektronnya, terutama pada jumlah valensinya. Unsur dengan jumlah valensi yang sama umumnya mempunyai kemiripan sifat. Untuk itu, sistem periodik unsur disusun berdasar pada kenaikan nomor atom & kemiripan sifat suatu zat.
Terdapat hubungan antara konfigurasi elektron atom unsur dengan letak unsur dalam sistem periodik, dimana:
- Nomor golongan sama dengan jumlah nilai valensi, kecuali untuk unsur He pada golongan VIIIA serta golongan transisi.
- Nomor periode sama dengan jumlah kulit pada elektron.
Konduktivitas Listrik
Elektron valensi juga memiliki tanggung jawab terhadap konduktivitas listrik sebuah unsur. Hal inilah yang membuat unsur dapat dikelompokan sebagai non logam, semikonduktor, dan logam. Unsur logam umumnya memiliki konduktivitas listrik yang tinggi apabila berada di dalam keadaan padat.
Pada setiap baris tabel periodik, logam terletak pada bagian sebelah kiri non logam. Sehingga logam memiliki jumlah valensi yang lebih sedikit daripada non logam.
Namun nilai valensi atom logam mempunyai energi ionisasi kecil dan pada keadaan padat, elektron ini relatif bebas untuk meninggalkan 1 atom atau untuk bergabung dengan atom lainnya.
Elektron bebas seperti ini bisa dipindahkan dengan pengaruh medan listrik, gerakannya dapat mengandung arus listrik. Elektron ini bertanggung jawab terhadap konduktivitas listrik logam. Contoh konduktor yang baik adalah aluminium, tembaga, emas, dan perak.
Unsur non logam mempunyai konduktivitas listrik yang rendah sehingga bertindak sebagai isolator. Unsur seperti ini bisa dilihat pada tabel periodik sebelah kanan dan mempunyai kelopak valensi sekurang-kurangnya setengah penuh.
Energi ionisasi dikatakan besar apabila elektron tidak bisa meninggalkan atom dengan mudah ketika berhadapan dengan medan listrik. Sejingga unsur semacam ini memiliki kemampuan menghantarkan arus sangat kecil.
Contoh unsur isolator pada antara lain adalah belerang dan intan. Senyawa padat yang mengandung logam bisa juga dikatakan isolator jika valensi atom logam digunakan untuk membentuk suatu ikatan ionik.
Baca: Mekanika Kuantum
Konfigurasi Elektron
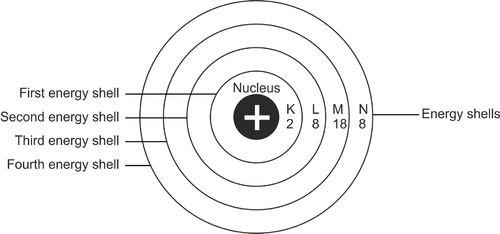
Proses konfigurasi bisa dikatakan sebagai susuban persebaran elektron dalam sebuah atom. Umumnya, elektron akan berada pada lintasan tertentu pada sebuah atom. Hal tersebut ditentukan berdasarkan level energi sebuah atom. Lintasan tersebut adalah kulit elektron.
Bagian pertama pada lapisan kulit dinotasikan dengan huruf K. Lapisan kulit akan berlanjut ke L, M, dan seterusnya sesuai alfabet. Kulit K berada paling dekat dengan inti atom. Setiap lapisan kulit hanya mampu menampung sejumlah elektron tertentu.
Sehingga jika sudah penuh, elektron akan berpindah ke lapisan selanjutnya. Semua lapisan kulit perlu diisi sebanyak kapasitas maksimalnya.
Cara Menghitung Elektron Valensi
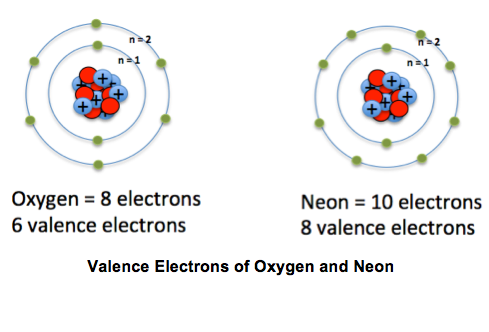
Posisi elektron ketika mulai mengisi bagian atom adalah dimulai dari kulit lapisan pertama terlebih dahulu. Lapisan kulit ini berada paling dekat dengan bagian inti atom atau dilambangkan dengan huruf K. Lapisan pertama memiliki tingkatan energi yang paling rendah. Jika lapisan pertama sudah terisi 2 elektron, maka akan dilanjutkan dengan mengisi lapisan selanjutnya yang disebut dengan L.
Kapasitas kulit L berjumlah 8 elektron. Jika sudah penuh akan dilanjutkan ke lapisan kulit berikutnya secara bertahap. Jumlah kapasitas kulit terluar pada atom adalah sebanyak 8 elektron.
Unsur yang termasuk dalam golongan utama, konfigurasi elektronnya bisa ditentukan berdasarkan jumlah elektron atau nomor atom sesuai dengan aturan berikut ini.
- Elektron akan terisi penuh hingga batas maksimal yang bisa ditampung oleh lapisan kulit.
- Jika masih terdapat elektron yang tersisa atau tidak dapat mengisi lapisan kulit elektron sampai ke batas maksimal, maka perhatikan ketentuannya berikut ini.
- Jika jumlah elektron yang tersisa > 32, maka bagian kulit selanjutkan diisi dengan 32 elektron
- Apabila elektron yang tersisa < 32, lapisan kulit selanjutnya akan menampung 18 elektron;
- Apabila elektron tersisa < 18, lapisan selanjutnya akan diisi 8 elektron.
- Jika jumlah tersisa ≤ 8, elektron yang masih tersedia dapat mengisi bagian kulit yang selanjutnya.
Baca: Perubahan Fisika
Contoh Soal Elektron Valensi

Agar dapat memahami materi secara lebih dalam, silahkan simak beberapa contoh dan pembahasan berikut ini.
Contoh 1
Tentukan nilai valensi unsur-unsur berikut berdasarkan konfigurasi elektronnya.
- 11Na
- 13Al
- 15P
- 18Ar
- 19K
Jawaban:
- 11Na = 2 8 1
Jumlah valensi Na = 1
- 13Al = 2 8 3
Jumlah valensi Al = 3
- 15P = 2 8 5
Jumlah valensi P = 5
- 18Ar = 2 8 8
Jumlah valensi Ar = 8
- 19K = 2 8 8 1
Jumlah valensi K = 1
Contoh 2
Buat konfigurasi elektron kemudian tentukan nilai valensi beberapa unsur berikut ini dengan menggunakan konfigurasi elektron gas mulia.
- 20Ca
- 35Br
- 36Kr
- 50Sn
- 86Rn
Jawaban:
- 20Ca = [Ar] 4s2
Jumlah nilai valensi Ca = 2
- 35Br = [Ar] 3d10 4s2 4p5
Jumlah nilai valensi Br = 7
- 36Kr = [Ar] 3d10 4s2 4p6
Jumlah nilai valensi Kr = 8
- 50Sn = [Kr] 4d10 5s2 5p2
Jumlah nilai valensi Sn = 4
- 86Rn = [Xe] 4f14 5d10 6s2 6p6
Jumlah nilai valensi Rn = 8
Contoh 3
Silahkan tulis elektron dari unsur-unsur di bawah ini dan tentukan juga nilai valensinya.
- 10 Ne
- 33 As
- 47 Ag
- 52 Te
- 54 Xe
Jawaban:
- 10 Ne: 1s2 2s2 2p6
Jumlah nilai valensi Ne = 8
- 33 As: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p3
Jumlah nilai valensi As = 5
- 47 Ag: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s1 4d10
Jumlah nilai valensi Ag = 1
- 52 Te: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p4
Jumlah nilai valensi Te = 6
- 54 Xe: 1s2 2s2 2p6 3s2 3p6 4s2 3d10 4p6 5s2 4d10 5p6
Jumlah nilai valensi Xe = 8
Elektron valensi bisa ditentukan berdasarkan lintasan ditentukan atau orbitnya menggunakan konfigurasi elektron. Meskipun terlihat cukup rumit, namun menguasai materi ini merupakan hal yang perlu dilakukan agar bisa mengerjakan soal dengan mudah.