Salah satu materi yang dibahas dalam Kimia adalah larutan penyangga yang berperan penting untuk menstabilkan pH, baik dalam tubuh maupun pada reaksi kimia tertentu. Larutan ini disebut juga dengan buffer atau larutan dapar.
Larutan buffer sering dimasukkan ke produk yang digunakan dalam kehidupan sehari-hari. Contoh sederhananya yakni obat tetes mata yang tidak menyebabkan rasa perih saat diteteskan ke mata. Bagaimana hal itu bisa terjadi? Berikut penjelasan rinci tentang larutan dapar.
Daftar Isi
Pengertian Larutan Penyangga

Larutan penyangga adalah larutan yang tidak mengalami perubahan kadar pH sama sekali jika ditambah air dan hanya mengalami sedikit perubahan jika dicampur dengan asam atau basa dalam kadar yang rendah.
Dengan kata lain, larutan yang disebut buffer ini memiliki kadar pH yang cenderung stabil walaupun terdapat cairan lain yang dimasukkan ke dalamnya. Contohnya, buffer dengan pH 5 akan tetap berada pada kadar yang sama setelah dicampur dengan air.
Buffer dengan pH 5 tersebut biasanya hanya akan berubah ke kadar 5,1 atau 4,9 setelah penambahan sedikit larutan asam atau basa. Jadi, tidak terjadi perubahan kadar pH menjadi terlalu tinggi atau terlalu rendah.
Sifat Larutan Penyangga

Cara yang mudah untuk mengenali dan membedakan buffer dengan jenis larutan lain yakni mengetahui sifat yang dimiliki. beberapa sifat khas dari buffer antara lain:
- Memiliki kemampuan untuk menjaga pH awal walaupun terjadi penambahan larutan lain seperti air, basa kuat atau asam kuat dengan kadar tertentu;
- Dapat mempertahankan pH awal walaupun larutan mengalami proses pengenceran;
- Kekuatan untuk menjaga pH akan semakin besar apabila memiliki jumlah mol yang banyak;
- Mampu mempertahankan nilai Ka, baik pada suhu yang sering berubah maupun suhu yang tetap.
Baca: Zat Cair
Prinsip Larutan Penyangga

Perlu diketahui bahwa buffer dikategorikan menjadi 2 jenis yakni larutan asam dan basa. Apa pengertiannya?
- Buffer asam adalah jenis larutan yang dibuat dari campuran asam lemah dan basa konjugasinya sehingga efektif untuk menjaga pH awal pada kondisi asam;
Contoh penyangga asam yaitu CH3COOH dan CH3COO– atau CH3COOH dan CH3COONa, HF dan NaF serta NaH2PO4 dan NaHPO4. - Buffer basa yaitu jenis larutan yang berasal dari basa lemah dan asam konjugasinya yang dicampur sehingga mampu menjaga pH awal pada kondisi basa.
Contoh penyangga basa yaitu N2H4 dan N2H5+ serta NH3 dan NH4+.
Asam dan basa yang dicampur dengan konjugasinya masing-masing akan memunculkan kesetimbangan ion dalam air. Alhasil, larutan buffer mampu menjaga pH tetap pada rentang tertentu tanpa mengalami perubahan yang banyak.
Lalu, bagaimana cara kerjanya? Berikut gambaran sederhananya untuk memperjelas:
- Apabila campuran basa lemah (NH4OH) dan asam konjugasinya ditambah dengan basa dalam kadar yang sedikit, maka akan terjadi reaksi yang dilakukan oleh ion OH– dan ion positif yang berasal dari asam konjugasi (NH4+);
- Apabila campuran asam lemah (CH3COOH) dan basa konjugasinya (CH3COO–) ditambah dengan larutan asam dalam kadar yang relatif kecil, maka akan terjadi reaksi antara ion H+ dan ion negatif yang berasal dari basa konjugasi (CH3COO–).
Baca: Stoikiometri
Fungsi Larutan Penyangga
Dalam kehidupan sehari-hari, buffer ternyata memiliki kegunaan yang sangat penting bagi manusia dan tumbuhan. Apa saja fungsi yang dimaksud?
- Bagi tumbuhan, buffer digunakan untuk menyeimbangkan kadar pH pada tanaman yang dibudidayakan memakai sistem hidroponik. Kadar pH yang seimbang akan berpengaruh baik pada perkembangan tanaman;
- Bagi manusia, buffer berperan untuk menjaga pH darah tidak berubah-ubah. Kadar pH dalam darah dijaga dengan baik sehingga proses metabolisme dalam tubuh berjalan dengan lancar. Jenisnya berupa buffer hemoglobin, buffer fosfat dan buffer karbonat;
- Bagi manusia, buffer masih memiliki fungsi lain yakni menjaga konsistensi kadar pH dalam mulut sehingga tidak menyebabkan kerusakan pada gigi. Larutan untuk mempertahankan pH tersebut dikeluarkan oleh air ludah sehingga asam dari makanan yang masuk ke mulut bisa dinetralkan.
Kapasitas Larutan Penyangga

Pada kenyataannya, larutan buffer memiliki kapasitas yang juga disebut dengan intensitas buffer atau indeks buffer. Kapasitas buffer yakni ukuran yang menunjukkan kemampuan buffer dalam menjaga konsistensi kadar pH saat dicampurkan dengan basa kuat atau asam kuat.
Intensitas buffer sangat dipengaruhi oleh jumlah kandungan basa-garam atau asam-garam dalam larutan masing-masing. Adapun larutan penyangga yang memiliki kapasitas terbesar adalah larutan yang memiliki kandungan asam-garam atau basa-garam berjumlah besar.
Misalnya, CH3COOH dan CH3COONa berjumlah 2 mol lebih besar kapasitasnya dibandingkan dengan kombinasi CH3COOH dan CH3COONa yang hanya berjumlah 1 mol.
Sedangkan jika kandungannya kecil, maka kapasitas buffer juga kecil. Indeks buffer yang kadarnya tinggi, maka akan bekerja lebih efektif untuk menetralkan asam atau basa sebelum terjadi perubahan pH yang signifikan.
Selain itu, kapasitas buffer juga dipengaruhi oleh perbandingan jumlah mol asam-garam atau basa-garam. Perbandingan yang besar, tentu menghasilkan buffer yang intensitasnya juga besar.
Misalnya, CH3COOH dan CH3COONa yang perbandingannya 1:1 (nilainya sama dengan 1) lebih besar dibandingkan CH3COOH dan CH3COONa yang perbandingannya 1:2 (nilainya menjadi 0,5).
Baca: Rumus Massa Jenis
Rumus Larutan Penyangga

Bagaimana penghitungan buffer? Terdapat rumus yang harus diterapkan untuk melakukan penghitungan tersebut. Rumus terbagi menjadi dua yakni khusus buffer asam dan buffer basa.
Pertama, rumus larutan penyangga asam sebagai berikut:

Ka merujuk pada tetapan dari kesetimbangan asam
V adalah valensi yang merupakan jumlah kandungan basa konjugasi atau ion yang lemah
Kedua, rumus larutan penyangga basa yaitu:
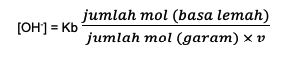
Kb merupakan tetapan dari kesetimbangan basa
V yakni valensi yang merupakan jumlah kandungan asam konjugasi atau ion yang lemah
Contoh Soal Larutan Buffer dan Pembahasannya

Berikut contoh soal untuk lebih mengasah pemahaman tentang buffer:
1. Larutan CH3COOH 0,1 M, Ka (10-5) sebanyak 200 ml ditambahkan ke dalam larutan CH3COONa 0,1 M sebanyak 200 ml juga, maka berapa pH campurannya?
Langkah yang pertama yakni menghitung mol setiap larutan terlebih dahulu:
Mol CH3COOH = m v = 0,1 200 = 20 mmol
Mol CH3COONa = m v = 0,1 200 = 20 mmol
Kemudian, langsung masuk ke dalam rumus buffer untuk penyangga asam:

Berdasarkan penghitungan tersebut, konsentrasi ion H+ sudah diketahui yakni . Selanjutnya masuk ke penghitungan untuk mencari pH, yakni:
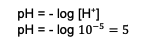
Jadi, pH campuran yang terjadi adalah 5.
2. Larutan NH3 0,1 M Kb (10-5) sebanyak 400 ml dicampur dengan larutan NH4Cl 0,1 M sebanyak 200 ml. Tentukan pH campuran yang muncul karena percampuran tersebut!
Tahap yang pertama yakni mengetahui mol larutan, yakni:
Mol NH3 = m v = 0,1 400 = 40 mmol
Mol NH4Cl = m v = 0,1 200 = 20 mmol
Setelah itu, gunakan rumus penyangga basa untuk mengetahui konsentrasi ion OH– yang akan dipakai untuk menghitung pH nantinya.
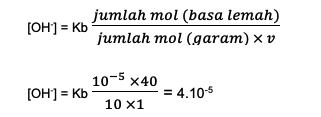
Kemudian, masuk ke penghitungan pH campuran yakni:
pOH = – log [OH–] = 5 – log 4
pH = 14 – pOH
pH = 14 – (5 – log 4) = 9 + log 4
Kesimpulan
Buffer merupakan larutan yang mampu menjaga kadar pH awal pada rentang tertentu setelah ditambah dengan sedikit larutan asam atau basa. Jenisnya ada 2 yakni penyangga asam dari asam lemah dan garamnya serta penyangga basa dari basa lemah dan garamnya.
Mempelajari tentang larutan penyangga yang memiliki fungsi dalam kehidupan merupakan hal yang penting. Tidak hanya memahami prinsip kerja, tetapi juga bisa mengetahui pH campuran dari buffer yang sudah terbentuk maupun pada reaksi asam-basa untuk membentuk buffer.